博文
谈谈LiTFSI和LiFSI在电解液中的应用
||
这两个盐都是酰亚胺类锂盐,具有共同的特点:溶解性极强,吸水后可以自溶解,水解速度慢,耐高温,一定的电压下对集流体有腐蚀性。
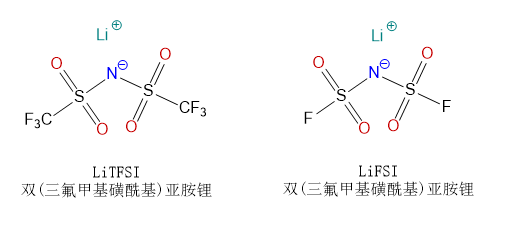
LiTFSI[90076-65-6]进入应用的时间比LiFSI[171611-11-3]要早很多年,我最早接触的LiTFSI是日本森田化工提供的样品,用于开发低温电解液,当时优化后的用量在1.5%左右,在溶剂中搭配羧酸酯EA,调低EC的含量,调高EMC含量,做出来的电解液低温效果非常好,-20℃放电当时的指标设定为80%,轻松通过. 后来,3M公司也推出了这个产品,名字为HQ-115,在行业内也得到了很多的认可。再后来还有罗地亚在国内生产此添加剂,目前国内做这个比较好的是国泰超威。当时美国同事喜欢把这个盐叫做“imide”,我对此颇有印象。
LiTFSI给我印象最深的就是:因为母体中心原子是带孤对电子的氮原子,一般胺类化合物都是弱碱性甚至是中强的碱性,比如三乙胺、氨 。但是当它连接的二个氢原子或烷基被吸电子的三氟甲基磺酰基(TFS)替代之后, 氨上的氢原子变得非常容易离解,HTFSI显示强酸性,完全来了个大翻转!从而导致LiTFSI是中性的。
根据类似的原理,如果将三氟甲基替换成同样是吸电子的但体积更小的氟原子(少了一个CF2),就得到了LiFSI。二个氟磺酰基(FSO2)连接到氮原子上,NH3分子变成了强酸性的HFSI,这是一种无色透明的油状液体,稍显粘稠。HFSI可以用来制备它的盐类,比如Mg(FSI)2, Fe(FSI)2,NaFSI等。 作为强酸强碱盐,它的锂盐LiFSI也是中性的。
LiFSI与LiTFSI对比,也就是这两个端基(F vs CF3)的差别上。 相比较而言,F-S键的稳定性要弱于C-S键,因此F-S键的水解速度更快,耐热能力也是F-S键不如C-S键。我之前做过对比,将LiFSI烘到100℃它会发生明显的变色,但LiTFSI是没有问题的。
但因为都是酰胺型锂盐,这两者都有良好的溶解能力,较好的耐水解能力和对温度的稳定性(vs LiPF6),但同时也都有腐蚀铝箔的能力。可能是由于F-S键相对更容易断裂一点,而断裂的氟对铝箔有一定的保护作用,因此LiFSI对铝箔进行腐蚀的开启电位要高一些, 在4.35V以上;而LiTFSI对铝箔在4.2V左右就不太稳定了。对铜箔这两者都是稳定的,没有腐蚀性。LiFSI还观察到过对不锈钢外壳的腐蚀,这个不知道是什么原因,LiTFSI没有这样的反映。此外,有文献报道过,LiPF6的存在可以帮助稳定铝箔,也就是LIPF6能够一定程度上钝化正极集流体,从而抑制LiTFSI或LiFSI的破坏作用。这也是为什么多数配方中都有LIPF6的原因。当然,你也可以寻找其它效果更好的钝化剂来配合亚胺锂盐的使用。
LiTFSI和LiFSI的溶解能力甚至让人吃惊,固态的锂盐甚至能够在空气中吸收水分,十几分钟所吸收的水分能让锂盐溶解在其中形成一滩溶液,速度十分迅速。由此也可见干燥这类锂盐时,需要严格保证密封性和干燥性,气氛稍有不好,就很难达到电解液所需要的水分标准(大约在200ppm以下)。这也是为什么之前有些厂家提供的200ppm以下水分的LiTFSI比高水分含量的LiTFSI贵得多的原因。由此也可以想到,除了水汽之外,LiTFSI或LiFSI也会对其它小分子溶剂的蒸汽有比较强的吸收能力,导致锂盐中混入其它溶剂。因此在操作LiTFSI或LiFSI的环境中,应避免不希望存在的溶剂蒸气被吸收而带来污染。
说到这里,我想起了两个花絮: 1) 用于FeS2-Li一次电池电解液的的碘化锂在脱水之前,LiI·3H2O释放的结晶水,能够将自己溶解。这个也挺特别的。 2)曾有过,溶剂的蒸气通过空间迁移重新溶解到另一杯电解液中,造成成分污染的案例。由此想到生产过程中如果易挥发的蒸气不管控,也可能造成蒸气污染。甚至在长年调配电解液的釜顶上,EC的蒸气形成的结晶结了厚厚的一层。这种意想不到的蒸气扩散造成的污染或意外,积累起来的效果也是不可小瞧的。
谈到具体的应用方面,LiTFSI曾经相当受重视,它能够提升电解液的电导率,作为少量的添加剂提升电解液的低温性能,但对高温性能的帮助却不明显。经过3M公司的多年推广,在一次电解液和二次电解液中都得到了应用。我当年还研究过用LiTFSI代替或部分代替LiI在锂-FeS2电池中的应用,可以提升电解液的大电流放电性能,效果不错。在二次电解液中,某大厂也曾批量在电解液中用LiTFSI,但最终还是因为成本过高等原因而放弃了应用。
再后来,随着LiFSI的流行,它具有与LiTFSI相似的特点和稍优一些的特性,使得LiTFSI迅速的被挤出了锂电电解液的市场。相反,LiFSI在这块市场迅速开花结果,几乎得到了所有大的电解液厂的认可与应用,甚至少见的出现了各家都不约而同的投入合成生产这种添加剂的少见现象。目前来讲,传统的液态电解液中已经基本上考虑采用LiFSI。在锂离子电池电解液中基本上看不到LiTFSI的量产应用了,但LiTFSI在聚合物中的良好分散能力与稳定性,使其在聚合物基质的电解质还有用途,或在一些固态电解质的研究中仍有应用。
在1~3%这个水平上的用量,一般是作为添加剂来看待的,LiFSI几乎可以用到所有类型的二次电解液中,三元/锂钴/磷酸铁锂都可,它与负极材料也没有什么不兼容的现象,高温下不容易分解产气,低温下电导率良好,溶解性好,各方面性能都比较好,没有显著的短板,成本上又在快速的下调之中,这样的添加剂不受欢迎才怪。不过出于成本考虑,一般在磷酸铁锂配方和钴锂配方中,比较少用LiFSI,大部分的应用还主要在三元电解液中。
浓度再高一些,3~5%这样的水平上,一般就把它看成是一种辅助的锂盐,这样的应用也有,在之前LIPF6价格比较低(8~12W/t)的正常时候,这种用法成本比较高,一般只在某些特别强调性能的电池上才舍得用。但现在LiPF6的价格猛涨的情况之下,反而LiFSI比它还便宜一点,这种用法的可能性就大了。不过话说回来,如果真的普遍这么用,LiFSI也存在供应不足的问题,与LiPF6相比LiFSI的产能要小得多得多,“易涨易退山溪水”,一旦这类应用爆发,价格可能涨得比LIPF6更快,这种优势又很快丧失了。因此从整体来看,我推测是LiFSI的应用比例会缓慢的上升,到某个浓度也就不再往上提了。
纯的LiFSI作为主盐的用法也是有的,由于对铝箔的腐蚀问题,在低电压的体系下比较放心,LiFSI在磷酸铁锂电池中是经过测试和验证的,循环性能不错。在三元材料中作为主盐还存在一些问题,实验数据表明有的体系用混合盐(LIPF6+LiFSI)的效果比较好.但换成纯的LiFSI性能反而下降,循环也变差了。因此这类应用可能还需要配合其它添加剂进行研究,特别是长循环下或电压偏高的情况下的性能研究,要慎重应用。
目前国内已经有很多的LiFSI生产厂家,生产工艺也各有不同,形成了比较好的竞争态势,相信在这样的情况下,LiFSI会得到更广泛的应用,其成本也会不断下降,应用比例也会相应的提升,在将来有希望发展成为一种重要的辅盐。
其它的酰亚胺锂盐

在中心氮原子上接上不同的酰基,就可以得到不同的锂盐。锂电中研究得比较多的是各种含氟烷基磺酰基的组合(常规烷基酰基连接形成的亚胺,其酸性不足,无法得到离解完全的锂盐) 。
先说对称性的酰亚胺锂盐,比如早期研究比较多的除了LiTFSI外,还有双(五氟乙基磺酰基)亚胺锂 LiBETI [132843-44-8] (它还有一个商品名Fluorad FC-130),它腐蚀铝箔的开启电位比LiTFSI高,抗水解性好,发表过一些文章,但这种盐非常昂贵,导致想买来测试也不太舍得,因此并没有实用。
再看看不对称的,(三氟甲基)(九氟丁基)磺酰亚胺锂[176719-70-3],它是一种不对称磺酰基亚胺锂盐类电解质,能有效抑制电解液的阳极氧化及Al自身的溶解反应,研究表明:此盐/EC/DMC在LiCoO2上和Al电极上的氧化电位均大于4.8V,且Al在该电解液体系中的阳极腐蚀被抑制。
(氟磺酰基)(三氟甲磺酰)亚胺锂 [192998-62-2] 缩写LiFTFSI,中央硝子的专利WO2021006238提到. 论文DOI:10.1016/j.jpowsour.2017.11.045报道对比过LiTFSI,LiFSI和LiFTFSI的特性。但一般来讲,这种不对称的磺酰亚胺锂盐,要往氮原子分别接上不同的基团,容易产生多种竞争结构,其提纯和收率估计比较困难,成本不低,如果没有找到合适的路线达到低廉的成本,就很难实用化。
最后看看环形的酰亚胺锂盐,由于螯合到氮原子上的环比一般的三氟甲基等要大一些,我推测,如果腐蚀形成的大分子的二酰亚胺铝盐在溶剂中不溶解,则可能沉积在电极表面阻碍进一步的腐蚀,实现动力学上的稳定。由此我们测试过 1,3-全氟丙二磺酰亚胺锂 [189217-62-7],根据实验测试结果显示,加入1.5%的这种锂盐不会对铝箔造成腐蚀,但其循环性能上还是不如LiFSI,因而没有进一步的开发。
https://blog.sciencenet.cn/blog-1213210-1306137.html
上一篇:电解液添加剂的结构联合形式
下一篇:分享一个计算分子量的Python小工具