博文
物质的摩尔定压热容与反应焓的客观性
|
本文拟结合基希霍夫公式,探讨摩尔定压热容(Cp,m)及任意温度下化学反应的标准摩尔反应焓
(ΔrHθm,T)的客观性,供参考.
摩尔定压热容(Cp,m)
物质的摩尔定压热容通常是指:恒压、有效功为0,且不发生化学反应及相变的前提下,单位物质的量的
某物质吸收(或释放)的热量随温度的变化率,可记为:
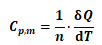 (1)
(1)
物质的摩尔定压热容可(设计实验)实测,数据客观真实.
2. 基希霍夫公式
基希霍夫公式可计算任意温度下,化学反应(或相变)的标准摩尔反应焓;其推导过程参见如下图(1):
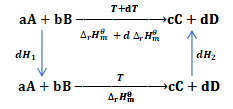
图1. 不同温度下化学反应“aA+bB→cC+dD”循环示意图
由图1可得: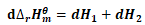 (2)
(2)
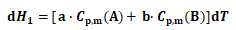 (3)
(3)
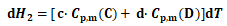 (4)
(4)
将式(3)、(4)代入式(2),取积分下限为298.15K, 并积分可得:
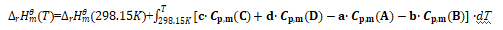 (5)
(5)
令: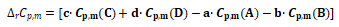 (6)
(6)
将式(6)代入式(5)可得:
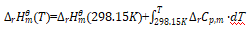 (7)
(7)
式(7)称基希霍夫公式.
3. 结果讨论
在 25℃、标态(或恒温恒压)下,化学反应“aA+bB→cC+dD”仅能通过范特霍夫平衡箱实现[1],
ΔrHθm(298.15K)、ΔrGθm(298.15K)及ΔrSθm(298.15K)均为虚拟数据[2].
尽管ΔrCp,m为真实数据,由基希霍夫公式所得ΔrHθm(T)仍是虚拟数据.
4. 结论
⑴ 物质的摩尔定压热容(Cp,m)数据客观真实;
⑵由基希霍夫公式计算所得ΔrHθm(T)为虚拟数据,不能实测.
参考文献
[1]余高奇. 反应进度(ξ)与热力学计算的虚拟性. 科学网博客,http://blog.sciencenet.cn/u/yugaoqi666.2021,4.
[2]余高奇.热力学数据源探究. 科学网博客,http://blog.sciencenet.cn/u/yugaoqi666.2021,8.
https://blog.sciencenet.cn/blog-3474471-1423477.html
上一篇:体积功对准静态过程假说的影响
下一篇:“恒温恒压”与“等温等压”两组概念的等效性探究